Les humains n'auraient pas existé sans virus car la protéine virale joue un rôle clé dans le développement de l'embryon humain. Cependant, ils constituent parfois des menaces existentielles sous la forme de maladies, comme dans le cas de la pandémie actuelle de COVID-19. Ironiquement, les virus représentent environ 8 % de notre génome, qui a été acquis au cours de l'évolution, ce qui fait de nous « pratiquement une chimère ».
Le mot le plus tristement célèbre et terrible de l'année 2020 est sans aucun doute 'virus'. Le roman coronavirus est responsable de l'actuelle maladie COVID-19 sans précédent et d'un quasi-effondrement de l'économie mondiale. Tout cela est causé par une minuscule particule qui n'est même pas considérée comme « pleinement » vivante car elle est dans un état non fonctionnel à l'extérieur de l'hôte, tout en ne se perpétuant à l'intérieur qu'en infectant l'hôte. Plus surprenant et choquant est le fait que le les humains portent les «gènes» viraux depuis des temps immémoriaux et actuellement, les gènes viraux constituent environ 8 % du génome humain (1). Pour mettre cela en perspective, seulement ~1% du génome humain est fonctionnellement actif, responsable de la fabrication de protéines qui déterminent qui nous sommes.
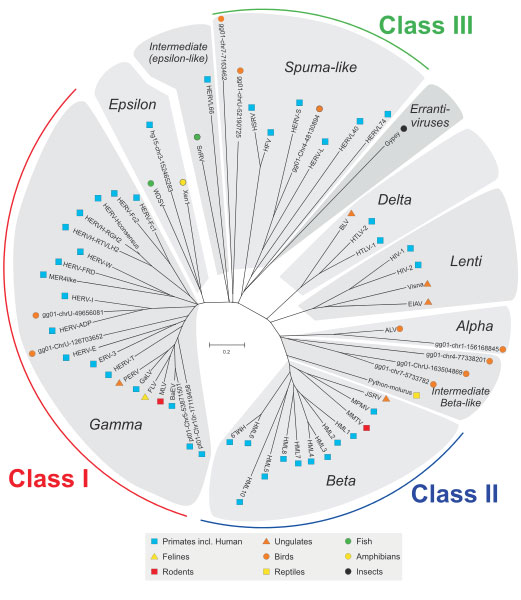
L'histoire de la relation entre les humains et virus a commencé il y a 20 à 100 millions d'années lorsque nos ancêtres ont été infectés par des virus. Chaque famille de rétrovirus endogènes est dérivée d'une infection unique des cellules germinales par un rétrovirus exogène qui, après s'être intégré à notre ancêtre, s'est développé et évolué (2). La propagation a suivi le transfert horizontal des parents à la progéniture et aujourd'hui, nous avons ces génomes viraux intégrés dans notre ADN en tant que rétrovirus endogènes humains (HERV). Il s'agit d'un processus continu et peut même se produire en ce moment. Au cours de l'évolution, ces HERV ont acquis des mutations, se sont stabilisées dans le génome humain et ont perdu leur capacité à provoquer la maladie. Les rétrovirus endogènes ne sont pas seulement présents chez l'homme mais sont omniprésents dans tous les organismes vivants. Tous ces rétrovirus endogènes regroupés en trois classes (classes I, II et III) présents dans différentes espèces animales présentent une relation phylogénétique basée sur leur similarité de séquence (3) comme le montre la figure ci-dessous. Les HERV appartiennent au groupe de classe I.
Parmi les différents rétrovirus incorporés présents dans le génome humain, un exemple classique qui mérite d'être mentionné ici est celui d'une protéine rétrovirale qui est une protéine d'enveloppe hautement fusogène appelée syncytine (5) dont la fonction originale dans le virus était de fusionner avec les cellules hôtes pour provoquer infection. Cette protéine a maintenant été adaptée chez l'homme pour former un placenta (fusion de cellules pour fabriquer des cellules multinucléées) qui non seulement fournit de la nourriture au fœtus de la mère pendant la grossesse, mais protège également le fœtus du système immunitaire de la mère en raison de la nature immunosuppressive de la syncytine. protéine. Ce HERV particulier s'est avéré bénéfique pour la race humaine en définissant son existence même.
Les HERV ont également été impliqués dans la fourniture d'une immunité innée à l'hôte en empêchant une nouvelle infection par des virus apparentés ou en réduisant la gravité de la maladie lors d'une réinfection par un type de virus similaire. Une revue de 2016 de Katzourakis et Aswad (6) décrit que les virus endogènes peuvent agir comme éléments régulateurs pour les gènes qui contrôlent la fonction immunitaire, conduisant ainsi au développement de l'immunité. La même année, Chuong et al (7) ont démontré que certains HERV agissent comme des activateurs de régulation en modulant l'expression de gènes inductibles par l'IFN (interféron) fournissant ainsi une immunité innée. Les produits d'expression HERV peuvent également agir comme des modèles moléculaires associés aux agents pathogènes (PAMP), déclenchant les récepteurs cellulaires responsables de la première ligne de défense de l'hôte (8-10).
Un autre aspect intéressant des HERV est que certains d'entre eux présentent des polymorphismes d'insertion, c'est-à-dire qu'un nombre différent de copies sont présentes dans le génome en raison d'événements d'insertion. Une étude de 20 sujets appartenant à différents groupes ethniques a révélé des modèles de polymorphisme d'insertion compris entre 0 et 87 % chez tous les sujets (11). Cela peut avoir des implications en provoquant des maladies par l'activation de certains gènes qui sont autrement silencieux.
Il a également été démontré que certains HERV sont associés au développement de troubles auto-immuns tels que la sclérose en plaques (12). Dans des conditions physiologiques normales, l'expression de HERV est étroitement régulée tandis que dans des conditions pathologiques dues à des changements dans l'environnement externe/interne, des changements hormonaux et/ou une interaction microbienne peuvent provoquer un dérèglement de l'expression de HERV, entraînant une maladie.
Les caractéristiques ci-dessus des HERV suggèrent que non seulement leur présence dans le génome humain est inévitable, mais qu'ils possèdent la capacité de réguler l'homéostasie du système immunitaire en l'activant ou en le supprimant, provoquant ainsi des effets différentiels (d'être bénéfique à provoquer une maladie) dans hôtes.
La pandémie de COVID-19 est également causée par un rétrovirus SARS-nCoV-2, qui appartient à la famille de la grippe, et il peut être plausible qu'au cours de l'évolution, des génomes liés à cette famille de virus se soient intégrés au génome humain et sont maintenant présents en tant que HERV. On suppose que ces HERV pourraient présenter des polymorphismes différents, comme mentionné ci-dessus, parmi des personnes d'origine ethnique différente. Ces polymorphismes peuvent se présenter sous la forme d'un nombre différentiel de copies de ces HERV et/ou de la présence ou de l'absence de mutations (modifications de la séquence du génome) accumulées sur une période de temps. Cette variabilité des HERV intégrés peut expliquer les taux de mortalité différentiels et la gravité de la maladie COVID-19 dans différents pays touchés par la pandémie.
***
Références:
1. Griffiths DJ 2001. Rétrovirus endogènes dans la séquence du génome humain. Génome Biol. (2001); 2(6) Avis 1017. DOI : https://doi.org/10.1186/gb-2001-2-6-reviews1017
2. Boeke, JD; Stoye, JP (1997). « Rétrotransposons, rétrovirus endogènes et évolution des rétroéléments ». Dans Coffin, JM; Hughes, SH; Varmus, HE (éd.). Rétrovirus. Presse de laboratoire Cold Spring Harbor. PMID 21433351.
3. Vargiu L, et al. Classification et caractérisation des rétrovirus endogènes humains ; les formes en mosaïque sont courantes. Rétrovirologie (2016) ; 13 : 7. DOI : 10.1186 / s12977-015-0232-y
4. Classes_of_ERVs.jpg : Jern P, Sperber GO, Blomberg J (œuvre dérivée : Fgrammen (talk)), 2010. Disponible en ligne sur https://commons.wikimedia.org/wiki/File:Classes_of_ERVs.svg Consulté le 07 mai 2020
5. Blond, JL; Lavillette, D; Cheynet, V; Bouton, O ; Oriol, G; Chapelle-Fernandes, S; Mandrandes, S; Maillet, F; Cosset, Floride (7 avril 2000). « Une glycoprotéine d'enveloppe du rétrovirus endogène humain HERV-W est exprimée dans le placenta humain et fusionne les cellules exprimant le récepteur du rétrovirus mammifère de type D ». J. Virol. 74 (7) : 3321-9. EST CE QUE JE: https://doi.org/10.1128/jvi.74.7.3321-3329.2000.
6. Katzourakis A et Aswad A. Evolution : les virus endogènes fournissent des raccourcis dans l'immunité antivirale. Biologie actuelle (2016). 26 : R427-R429. http://dx.doi.org/10.1016/j.cub.2016.03.072
7. Chuong EB, Elde NC et Feschotte C. Évolution régulatrice de l'immunité innée par cooptation de rétrovirus endogènes. Sciences (2016) Vol. 351, numéro 6277, pages 1083-1087. EST CE QUE JE: https://doi.org/10.1126/science.aad5497
8. Wolff F, Leisch M, Greil R, Risch A, Pleyer L. L'épée à double tranchant de la (ré)expression des gènes par des agents hypométhylants : du mimétisme viral à l'exploitation comme agents d'amorçage pour la modulation ciblée des points de contrôle immunitaire. Signal de communication cellulaire (2017) 15:13. EST CE QUE JE: https://doi.org/10.1186/s12964-017-0168-z
9. Hurst TP, Magiorkinis G. Activation de la réponse immunitaire innée par les rétrovirus endogènes. J Gen Virol. (2015) 96:1207-1218. EST CE QUE JE: https://doi.org/10.1099/vir.0.000017
10. Chiappinelli KB, Strissel PL, Desrichard A, Chan TA, Baylin SB, Correspondence S. L'inhibition de la méthylation de l'ADN provoque une réponse d'interféron dans le cancer via l'ARNdb, y compris les rétrovirus endogènes. Cell (2015) 162:974-986. EST CE QUE JE: https://doi.org/10.1016/j.cell.2015.07.011
11. Mehrab G, Sibel Y, Kaniye S, Sevgi M et Nermin G. Dépistage d'insertion de rétrovirus-H endogène humain. Rapports de médecine moléculaire (2013). EST CE QUE JE: https://doi.org/10.3892/mmr.2013.1295
12. Gröger V et Cynis H. Rétrovirus endogènes humains et leur rôle putatif dans le développement de troubles auto-immuns tels que la sclérose en plaques. Microbiol avant. (2018); 9 : 265. DOI : https://doi.org/10.3389/fmicb.2018.00265
***