Les « systèmes CRISPR-Cas » dans les bactéries et les virus identifient et détruisent les séquences virales envahissantes. C'est un système immunitaire bactérien et archéen pour la protection contre les infections virales. En 2012, le système CRISPR-Cas a été reconnu comme un génome outil d'édition. Depuis lors, une large gamme de systèmes CRISPR-Cas ont été développés et ont trouvé des applications dans des domaines tels que la thérapie génique, le diagnostic, la recherche et l'amélioration des cultures. Cependant, les systèmes CRISPR-Cas actuellement disponibles ont une utilisation clinique limitée en raison des occurrences fréquentes d'éditions hors cible, de mutations inattendues de l'ADN et de problèmes héréditaires. Les chercheurs ont récemment signalé un nouveau système CRISPR-Cas capable de cibler et de détruire l'ARNm et protéines associés à différentes maladies génétiques avec plus de précision, sans impact hors cible ni problèmes héréditaires. Nommé Craspase, c'est le premier système CRISPR-Cas qui montre de protéines fonction d'édition. C'est également le premier système capable d'éditer à la fois l'ARN et de protéines. Parce que Craspase surmonte de nombreuses limitations des systèmes CRISPR-Cas existants, il a le potentiel de révolutionner la thérapie génique, le diagnostic et la surveillance, la recherche biomédicale et l'amélioration des cultures.
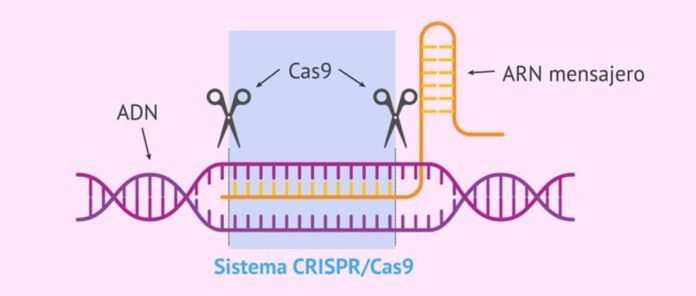
Le « système CRISPR-Cas » est le système immunitaire naturel des bactéries et des archées contre les infections virales qui identifie, lie et dégrade les séquences du gène viral à protéger. Il se compose de deux parties : l'ARN bactérien transcrit à partir du gène viral incorporé dans le génome bactérien après la première infection (appelé CRISPR, il identifie les séquences cibles des gènes viraux envahisseurs) et un destructeur associé. de protéines appelé « CRISPR associé de protéines (Cas) » qui lie et dégrade les séquences identifiées dans le gène viral pour protéger les bactéries contre les virus.
CROQUANT signifie « répétitions palindromiques courtes et régulièrement espacées ». Il s’agit d’ARN bactérien transcrit caractérisé par des répétitions palindromiques.
Les répétitions palindromiques (CRISPR) ont été découvertes pour la première fois dans les séquences de E. coli en 1987. En 1995, Francisco Mojica a observé des structures similaires chez les archées, et c'est lui qui a le premier pensé à celles-ci comme faisant partie du système immunitaire des bactéries et des archées. En 2008, il a été démontré expérimentalement pour la première fois que la cible du système immunitaire des bactéries et des archées était l’ADN étranger et non l’ARNm. Le mécanisme d'identification et de dégradation des séquences virales suggère que de tels systèmes pourraient être utilisés comme outils pour édition du génome. Depuis sa reconnaissance comme outil d’édition du génome en 2012, le système CRISPR-Cas a parcouru un très long chemin en tant que norme fermement établie. édition de gènes système et a trouvé un large éventail d’applications dans la biomédecine, l’agriculture et les industries pharmaceutiques, y compris dans la thérapie génique clinique1,2.
Une grande sélection d’ CRISPR-Des systèmes Cas sont déjà identifiés et actuellement disponibles pour la surveillance et l'édition de séquences d'ADN/ARN à des fins de recherche, de dépistage de médicaments, de diagnostics et de traitements. Les systèmes CRISPR/Cas actuels sont divisés en 2 classes (Classes 1 et 2) et six types (Type I à XI). Les systèmes de classe 1 ont plusieurs Cas protéines qui doivent former un complexe fonctionnel pour se lier et agir sur leurs cibles. En revanche, les systèmes de classe 2 n'ont qu'un seul grand Cas de protéines pour lier et dégrader les séquences cibles, ce qui rend les systèmes de classe 2 plus faciles à utiliser. Les systèmes de classe 2 couramment utilisés sont Cas 9 Type II, Cas13 Type VI et Cas12 Type V. Ces systèmes peuvent avoir des effets collatéraux indésirables, c'est-à-dire un impact hors cible et une cytotoxicité.3,5.
Thérapies géniques basés sur les systèmes CRISPR-Cas actuels ont une utilisation clinique limitée en raison des occurrences fréquentes d'éditions hors cible, de mutations inattendues de l'ADN, y compris des suppressions de fragments d'ADN importants et de grandes variantes structurelles de l'ADN au niveau des sites cibles et hors cible, entraînant la mort cellulaire. et d'autres problèmes héréditaires.
Craspase (ou caspase guidée par CRISPR)
Les chercheurs ont récemment signalé un nouveau système CRISPER-Cas, un système Cas2-7 de classe 11 de type III-E associé à un système de type caspase. de protéines donc nommé Craspase ou caspase guidée par CRISPR 5 (Les caspases sont des protéases à cystéine qui jouent un rôle clé dans l'apoptose en dégradant les structures cellulaires). Il a des applications potentielles dans des domaines tels que la thérapie génique et le diagnostic. Craspase est guidée et ciblée par l'ARN et n'intervient pas dans les séquences d'ADN. Il peut cibler et détruire l'ARNm et protéines associés à différentes maladies génétiques avec plus de précision sans impact hors cible. Ainsi, l’élimination des gènes associés aux maladies est possible par clivage au niveau de l’ARNm ou des protéines. En outre, lorsqu'elle est liée à une enzyme spécifique, la Craspase peut également être utilisée pour modifier les fonctions des protéines. Lorsque ses fonctions RNase et protéase sont supprimées, la Craspase devient désactivée (dCraspase). Il n’a pas de fonction de coupure mais se lie aux séquences d’ARN et de protéines. Par conséquent, dCraspase peut être utilisé en diagnostic et en imagerie pour surveiller et diagnostiquer des maladies ou des virus.
Craspase est le premier système CRISPR-Cas qui présente une fonction d'édition de protéines. C’est également le premier système capable d’éditer à la fois l’ARN et les protéines. C'est édition de gènes la fonction s’accompagne d’effets hors cible minimes et d’aucun problème héréditaire. Par conséquent, Craspase est probablement plus sûr en termes d’utilisation clinique et thérapeutique que les autres systèmes CRISPR-Cas actuellement disponibles. 4,5.
Parce que Craspase surmonte de nombreuses limitations des systèmes CRISPR-Cas existants, il a le potentiel de révolutionner la thérapie génique, le diagnostic et la surveillance, la recherche biomédicale et l'amélioration des cultures. Des recherches supplémentaires sont nécessaires pour développer un système d'administration fiable pour cibler avec précision les gènes responsables de maladies dans les cellules avant de prouver l'innocuité et l'efficacité dans les essais cliniques.
***
Références:
- Gostimskaya, I. CRISPR-Cas9 : Une histoire de sa découverte et des considérations éthiques de son utilisation dans l'édition du génome. Biochimie Moscou 87, 777–788 (2022). https://doi.org/10.1134/S0006297922080090
- Chao Li et al 2022. Outils et ressources informatiques pour l'édition du génome CRISPR/Cas. Génomique, protéomique et bioinformatique. Disponible en ligne le 24 mars 2022. DOI : https://doi.org/10.1016/j.gpb.2022.02.006
- van Beljouw, SPB, Sanders, J., Rodríguez-Molina, A. et al. Systèmes CRISPR-Cas ciblant l'ARN. Nat Rev Microbiol 21, 21–34 (2023). https://doi.org/10.1038/s41579-022-00793-y
- Chunyi Hu et al 2022. Craspase est une protéase activée par l'ARN et guidée par l'ARN CRISPR. Science. 25 août 2022. Vol 377, numéro 6612. pp. 1278-1285. EST CE QUE JE: https://doi.org/10.1126/science.add5064
- Huo, G., Shepherd, J. & Pan, X. Craspase : un nouvel éditeur de gènes double CRISPR/Cas. Génomique fonctionnelle et intégrative 23, 98 (2023). Publié : 23 mars 2023. DOI : https://doi.org/10.1007/s10142-023-01024-0
***